Микробная трансглютаминаза, ее коммерческие формы и методы контроля в пищевых добавках и готовой продукции
Мы с вами как рядовые потребители привыкли воспринимать пищевую индустрию как достаточно простой процесс, масштабируя наш опыт готовки на кухне на промышленные масштабы – большая мясорубка, большой блендер, большая печка, большой холодильник и прочее. При этом мы продолжаем рост требований к срокам годности, качеству и уникальности продуктов, вынуждая производителей изучать свой продукт досконально, понимать не только механику процесса, но и его биохимию – как сочетаются в продукте белки, жиры и углеводы, как на них влияет термическая обработка, каким образом можно поднять влагоудерживающие свойства продукта, как соединить в стабильный комплекс различное сырье.
Первоначально ответы строились на максимизации свойств самого сырья – использование дополнительной клейковины в тесте позволяло производить стабильную выпечку с не зерновыми включениями, добавление изолятов сои, гидроколлоидов и грамотная работа с фосфатами поднимали выход мясных продуктов, подобранные режимы посола рыбы позволяли получать структуру, подобную сашими, однако всегда казалось, что можно получить больше эффекта. Замедление эволюции пищевой промышленности привело к активным изучениям биохимических преобразований внутри тех или иных продуктов. Биохимики обратили внимание на естественный структурообразователь – тканевую трансглютаминазу (известную как pTG, tTG, TG1, TG2, фактор свертывания крови XIII и другие), отвечающую в нашем организме за стабилизацию и организацию сложных взаимодействий тканей (соединение между собой отдельных клеток в многоклеточные ткани), процессы заживления ран и процессы обновления клеток организма. У tTG есть естественный ограничитель – для запуска ее работы нужен свободный кальций, который в норме внутри организма в дефиците и выдается дозированно только для осуществления биохимических процессов. Тканевая трансглютаминаза встречается повсеместно – в тканях животных, растений, грибов [1].
Сходный продукт нашелся в микробиальном мире – бактерии Streptomyces mobaraensis (а также Streptomyces ladakanum, Streptomyces lividans, Bacillus spp., Actinomycetes) способны производить специфичный белок, который после выхода из клетки микроба активируется его бактериальной протеазой, превращаясь в активный фермент – микробную трансглютаминазу. Микробная трансглютаминаза (MTGase) – фермент класса трансфераз (EC 2.3.2.13), катализирующий образование ковалентных поперечных связей между белковыми молекулами. Основная реакция заключается в образовании ε-(γ-глутамил)лизиновых изопептидных связей между γ-карбоксамидной группой остатка глутамина и ε-аминогруппой остатка лизина в белках или пептидах [2]. Микробный фермент значительно меньше по молекулярному весу, чем тканевая трансглютаминаза, за счет чего он быстрее распределяется по объему пищевого продукта и приступает к своей работе – разрешению оригинального белка и формированию новых термонеобратимых связей. У фермента MTGase широкий диапазон доступных субстратов – он одинаково хорошо работает с мышечными белками (актин и миозин), казеином, белками бобовых, клейковиной, белками плазмы, белками яиц и многими другими. Чем выше содержание глутамина и лизина, тем большее количество связей образуется в продукте.
В результате ферментативной реакции происходит сшивание белковых молекул, что приводит к изменению их функциональных свойств:
- увеличению вязкости;
- повышению гелеобразующей способности;
- улучшению водоудерживающей способности;
- формированию прочной белковой сети [3].
По сути, трансглютаминаза действует как катализатор формирования новых связей между отдельными молекулами белка, в том числе тех, которые в норме никогда бы не сформировались. Поэтому в пищевой промышленности MTGase часто называют «фермент, сшивающий белки» или «мясной клей» [4].
Микробная трансглютаминаза формирует формирует изопептидные связи с образованием термонеобратимой ε-(γ-глутамил)лизиновой связи. В виде формулы этот процесс выглядит так: Gln–CONH2+Lys–NH2→Gln–CO–NH–Lys+NH3. Такие связи формируют внутримолекулярные и межмолекулярные сшивки, приводящие к полимеризации белков и образованию пространственной белковой сети. Именно эта функция mTGase наиболее интересна для применения в пищевой промышленности – получившиеся трехмерные структуры помимо придания плотности продукту также обладают повышенной эмульгирующей и влагоудерживающей способностью [5].
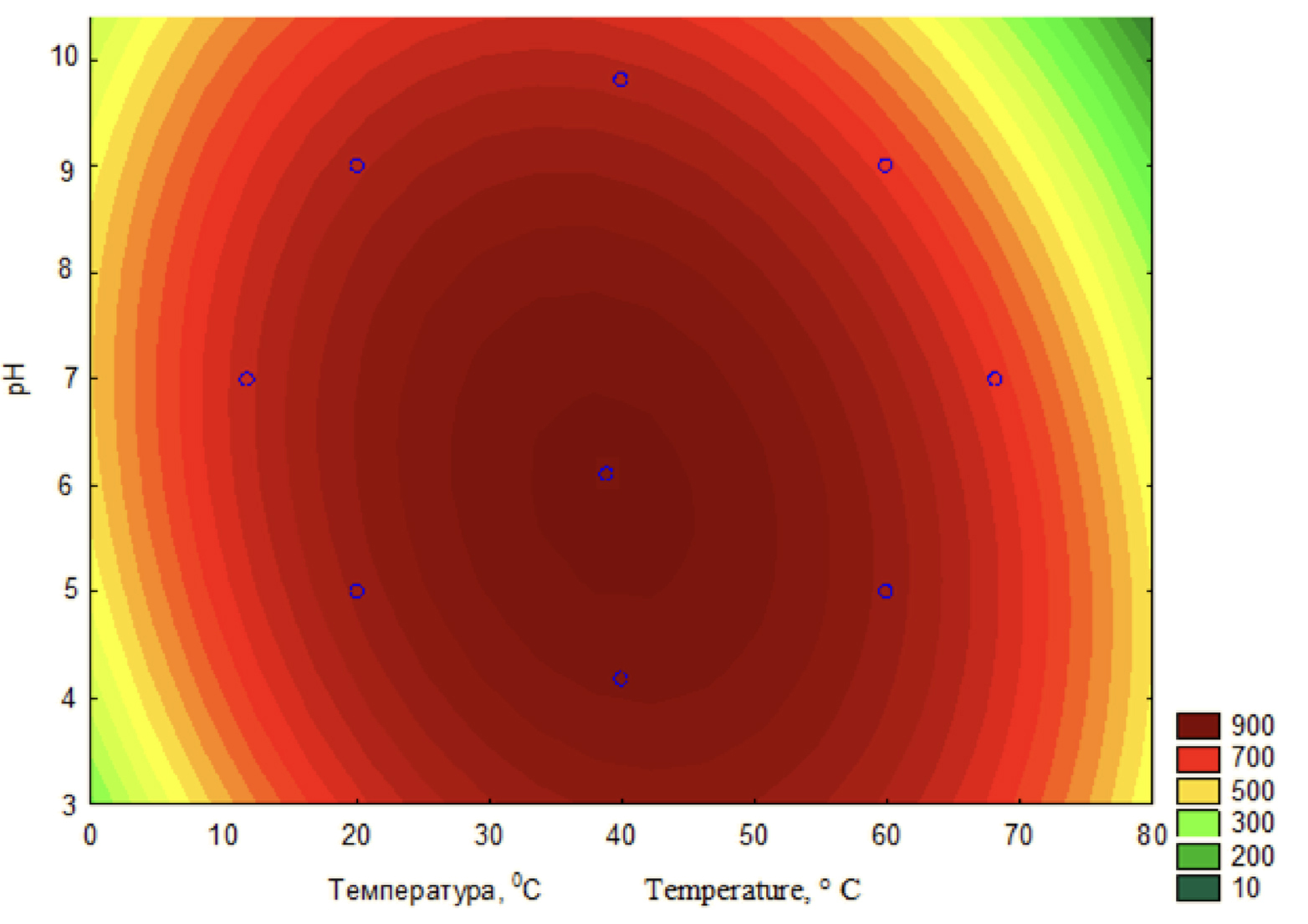
Как и у многих других биологических энзимов, у микробной трансглютаминазы есть допустимые и оптимальные технологические режимы. Фермент из Streptomyces mobaraensis демонстрирует максимальную активность при pH ~6 и температуре около 48 °C [6,7]. Для проведения реакции с белками мяса или рыбы необходимо наличие соли, которая ускоряет солюбизацию белка, повышая его доступность для фермента.
Диаграмма зависимости активности препарата мТг от уровня рН и температуры [6]
Для безопасности конечного потребителя важно, чтобы в готовом продукте фермент не проявлял остаточной активности и полностью разрушился пищеварительными ферментами. Ряд авторов [6, 8, 9] указывали в качестве температуры инактивации значения 60-80°С. Тем не менее, стоит отметить, что инактивация происходит не мгновенно (даже при +80°С требуется не менее 1 минуты), при этом, высокое содержание жира и низкая активность воды в продукте дополнительно замедляют процесс инактивации фермента. Таким образом, при недостаточной экспозиции фермент может сохранить свою активность в готовой продукции и негативно сказаться на здоровье потребителя. Несмотря на статус GRAS в США и наличия разрешения использования в качестве технологического фермента в некоторых странах ЕС, mTG остается недостаточно изученным ферментом. Влияние тканевой трансглутаминазы на развитие аутоиммунных заболеваний (например, целиакии) – одна из основных тем исследований, проводимых различными научными центрами по всему миру [4,11,12]. Это аутоиммунное заболевание, связанное с реакцией иммунной системы на глиадин (компонент белка плшеницы глютена). Доказано, что заболевание протекает за счет работы собственной трансглютаминазы организма – tTG, который модифицирует пептиды глиадина, полученные из глютена, образуя белковые структуры, которые иммунная система воспринимает как чужеродные. Кроме того, употребление белков, связанных с глютеном, таких как гордеин из ячменя, секалин из ржи или авенин из овса, может вызывать аналогичные воспалительные реакции в организме человека. Глиадин – мощный иммунотоксический агент, который может нарушать формирование межклеточных контактов в эпителиальных клетках. Роль привнесенной микробной трансглютаминазы описывается либо через образование комплексов глиадин-MTGase, либо формирование новых антигенов (в том числе за счет проведения реакции дезаминирования белка), либо усиливание иммунного ответа у людей с целиакией [4, 5]. Кроме того, mTGase может повышать проницаемость кишечника [10], что еще больше способствует проникновению антигенов и может повышать риск пищевой гиперчувствительности.
В промышленности mTGase представлена в нескольких коммерческих формах. Наиболее распространенная – нормализация фермента по активности до 100 условных единиц добавлением мальтодекстрина. Компания Ajinomoto, выпускающая mTG с торговой маркой Activa, добавляет в некоторых решениях к ферменту начальный белковый субстрат в виде казеинатов, КМБ, КСБ, соевых белков или глютена в зависимости от продукта, для которого будет использоваться комплекс. Основной негативной особенностью комплексных добавок и нормализованного фермента остается потеря активности энзима при хранении при положительных температурах и при доступе кислорода [13]. В качестве способов стабилизации производители предложили капсулировать фермент в барьерную полимерную или белково-полисахаридную матрицу, формируя микрочастицы (обычно 1–1000 µm), разрушающиеся под действием влаги продукта или при нагревании. Наиболее распространённые оболочки – казеинаты, желатин, гуммиарабик, мальтодекстрин, альгинаты, хитозан, липидные матрицы. Микрокапсулирование часто применяется для сохранения активности фермента при технологических воздействиях (сушка, окисление, колебания pH) – капсула стабилизирует третичную структуру фермента и уменьшает денатурацию при сушке. Помимо сохранения активности фермента в неблагоприятных условиях, подобное капсулирование позволяет регулировать активность фермента в продукте, предотвращая переуплотнение белковой сетки продуктов с длительной технологической экспозицией перед термообработкой [14, 15]. Ряд компаний, работающих на российском рынке, утверждают, что подобная технология также способствует маскировке mTGase в составе КПД и в готовой продукции, что позволяет обойти ограничения ТР ТС 021/2011 и ТР ТС 029/2012. Тем не менее, микрокапсулирование не изменяет принципиальной структуры белка (в противном случае нарушится структура активного центра и фермент потеряет протеолитическую либо «сшивающую» способность), фермент высвобождается из капсулы внутри обрабатываемого продукта и может быть выявлен в готовой продукции в активной либо инактивированной формах.
Лабораторный контроль микробной трансглютаминазы в пищевой продукции
Расширение применения микробной трансглютаминазы (mTG) в пищевой промышленности закономерно приводит к необходимости разработки надежных методов лабораторного контроля данного фермента в сырье, пищевых ингредиентах и готовой продукции. Особую сложность аналитического выявления представляет тот факт, что современные коммерческие формы фермента могут содержать различные стабилизирующие компоненты, включая белковые субстраты, носители и системы микрокапсулирования, которые способны существенно затруднять его обнаружение стандартными аналитическими методами.
В последние годы для контроля белковых технологических ферментов всё более широкое распространение получают иммунологические методы анализа, в частности иммуноферментный анализ (ИФА). Данный подход основан на высокоспецифическом взаимодействии антиген–антитело и позволяет выявлять белковые молекулы с высокой чувствительностью даже в сложных пищевых матрицах.
Российским разработчиком методов контроля качества и безопасности пищевых продуктов – компанией «Хема» совместно с Ростовским референтным центром Россельхознадзора разработаны специализированные ИФА-тест-системы для выявления микробной трансглютаминазы в пищевых продуктах, пищевых добавках и технологических ингредиентах. Метод основан на использовании высокоспецифичных антител к микробной трансглютаминазе Streptomyces spp., что обеспечивает селективное обнаружение фермента независимо от формы его технологического применения.
Ключевой особенностью разработанных тест-систем является возможность выявления:
- свободной микробной трансглютаминазы;
- фермента, стабилизированного белковыми субстратами (казеинаты, соевые белки, глютен и др.);
- фермента в составе комплексных пищевых добавок;
- микрокапсулированных форм микробной трансглютаминазы, используемых для повышения стабильности фермента и регулирования его активности в продукте.
Наличие микрокапсулированных форм фермента представляет отдельную аналитическую проблему. Полимерные, белково-полисахаридные или липидные оболочки способны препятствовать эффективному извлечению фермента из образца и снижать чувствительность анализа. Для решения данной задачи специалистами компании «Хема» была разработана специальная процедура пробоподготовки, включенная в последнюю версию методики ИФА.
Данная пробоподготовка обеспечивает:
- разрушение микрокапсульных оболочек;
- эффективную экстракцию фермента из белковых и технологических матриц;
- высвобождение фермента из стабилизирующих комплексов.
Это позволяет выявлять микробную трансглютаминазу даже в случаях, когда производители используют технологии микрокапсулирования или комплексные белковые носители.
За годы практического применения методика ИФА «Хема» показала высокую воспроизводимость результатов и устойчивость к различным пищевым матрицам. В настоящее время данные тест-системы широко используются в лабораторной практике и применяются более чем в 100 лабораториях, включая лаборатории системы государственного контроля, в том числе Роспотребнадзора и Россельхознадзора. Накопленный опыт применения подтверждает аналитическую надежность и практическую эффективность данного метода для мониторинга безопасности пищевой продукции. Дополнительным подтверждением аналитической надежности методики являются результаты сличительных (межлабораторных) испытаний, проведённых с участием профильных лабораторий. В рамках данных исследований было показано, что ИФА-методики «Хема» обеспечивают высокую воспроизводимость и сопоставимость результатов при анализе различных типов пищевых матриц. Полученные данные продемонстрировали стабильность выявления микробной трансглютаминазы, в том числе при низких концентрациях и в сложных технологических формах, включая микрокапсулированные препараты.
Результаты сличительных испытаний подтвердили корректность методики, её устойчивость к вариациям пробоподготовки и оборудования, а также возможность применения в рамках рутинного лабораторного контроля. Это дополнительно свидетельствует о высокой степени верификации метода и его пригодности для использования в системе государственного и производственного контроля безопасности пищевой продукции.
Регуляторные аспекты применения микробной трансглютаминазы
Использование микробной трансглютаминазы в пищевой промышленности регулируется законодательством различных стран и международных объединений. В странах Евразийского экономического союза вопросы безопасности пищевых продуктов регулируются техническими регламентами ТР ТС 021/2011 «О безопасности пищевой продукции» и ТР ТС 029/2012 «Требования безопасности пищевых добавок, ароматизаторов и технологических вспомогательных средств», которые предусматривают необходимость контроля используемых технологических ингредиентов и обеспечения прозрачности состава продукции.
В ряде стран использование микробной трансглютаминазы также вызывает активные научные и регуляторные дискуссии. В частности, в Китае применение фермента требует обязательного декларирования в составе продукта, а в Швейцарии и ряде стран Европейского союза введены дополнительные требования к маркировке продукции, содержащей технологические ферменты. В отдельных сегментах пищевой промышленности применение фермента может быть ограничено или требовать специального разрешения.
Подобные регуляторные подходы связаны с необходимостью обеспечения прозрачности пищевых технологий и информирования потребителей о составе продуктов.
Развитие биотехнологических методов модификации белков в пищевой промышленности открывает новые технологические возможности, однако одновременно повышает требования к прозрачности состава продукции и лабораторному контролю применяемых ферментных препаратов. Микробная трансглютаминаза является одним из наиболее активно используемых технологических ферментов, способных существенно изменять структурные свойства белковых систем и функциональные характеристики пищевых продуктов. Зарубежная и, в меньшей степени, отечественная научная периодика описывает множество решений по применению микробиальной трансглютаминазы для пищевой промышленности. Несмотря на то, что фермент микробиального происхождения, также называемый в просторечии «мясной клей», применялся изначально при только производстве сурими и соединения мясных и рыбных изделий, основным каналом продаж стала молочная промышленность, в которой фермент зачастую остается в продукте в активной форме. Достаточно распространена попытка применять его и в хлебопечении как для стабилизации структуры продукта, так и для выпуска безглютеновой продукции или продукции со сниженным содержанием пшеничной муки, замещая традициооные для этой отрасли ферменты-оксидазы.
Современные технологические решения, включая стабилизацию фермента белковыми субстратами и микрокапсулирование, могут существенно усложнять аналитическое выявление фермента. В этих условиях особое значение приобретают высокочувствительные иммунологические методы анализа. Использование ИФА-методик позволяет эффективно выявлять в готовой продукции микробную трансглютаминазу, внесенную в различных технологических формах (сухой, жидкой, капсулированной), выявлять даже следовые количества фермента (менее 10 единиц активности фермента на 100 кг продукта) и обеспечивает надежный лабораторный контроль содержания фермента в пищевой продукции.
Таким образом, несмотря на кажущееся удобство и простоту применения микробной трансглютаминазы, не стоит забывать о потенциальны рисках для здоровья потребителей и том факте, что современные методы контроля фальсификаций являются важным элементом обеспечения прозрачности пищевых технологий, соблюдения требований технических регламентов и защиты интересов потребителей. В любом продукте необходимый потребителю технологический эффект может быть достигнут легальным путем – за счет качественной работы с сырьевыми материалами, использования подготовленных белков (изолятов и гидролизатов), влиящих на реологию о органолептику продукта, ввода комплексных пищевых добавок и подбора оптимальных технологических параметров.
Список литературы:
- Т.Н. Пивненко Применение трансглутаминазы в пищевой промышленности Научные труды Дальрыбвтуза. 2021. № 1 (т. 55) с. 5-22
- Properties and applications of microbial transglutaminase. K Yokoyama, N Nio, Y Kikuchi // Appl Microbiol Biotechnol. 2004 May;64(4):447-54. doi: 10.1007/s00253-003-1539-5. Epub 2004 Jan 22 https://pubmed.ncbi.nlm.nih.gov/14740191/
- Microbial transglutaminase production: understanding the mechanism. Dongxu Zhang, Yang Zhu, Jian Chen // Biotechnol Genet Eng Rev. 2010:26:205-22. doi: 10.5661/bger-26-205.
- Processed Food Additive Microbial Transglutaminase and Its Cross-Linked Gliadin Complexes Are Potential Public Health Concerns in Celiac Disease Aaron Lerner and Torsten Matthias // Int. J. Mol. Sci. 2020, 21(3), 1127; https://doi.org/10.3390/ijms21031127 https://www.mdpi.com/1422-0067/21/3/1127
- Microbial transglutaminase in food biotechnology: from biochemical mechanisms to industrial applications Marek Kieliszek // Appl Microbiol Biotechnol. 2026 Jan 24;110(1):38. doi: 10.1007/s00253-025-13697-7 https://pmc.ncbi.nlm.nih.gov/ articles/PMC12835111
- Глотова И.А. Подходы к получению и применению микробной трансглутаминазы в эмульгированных мясо-растительных системах // И.А. Глотова, Е.Е. Курчаева, Е.Ю. Ухина, А.О. Рязанцева. Вестник ВГУИТ/Proceedings of VSUET, Т. 79, № 4, 2017 с.210-219.
- Purification and characterization of a high-salt-resistant microbial transglutaminase from Streptomyces mobaraensis Mingfei Jin, Jinge Huang, Zhengpei Pei et al., Journal of Molecular Catalysis B: Enzymatic Volume 133, November 2016, Pages 6-11 https://doi.org/10.1016/j.molcatb.2016.07.005 https://www.sciencedirect.com/ science/article/abs /pii/S1381117716301205
- Thermal stability and conformational changes of transglutaminase from a newly isolated Streptomyces hygroscopicus Li Cui, Guocheng Du, Dongxu Zhang, Jian Chen // Bioresource Technology. Volume 99, Issue 9, June 2008, Pages 3794-3800 https://doi.org/10.1016/ j.biortech.2007.07.017
- Characterisation and optimisation of microbial production of transglutaminase produced by Streptoverticillium cinnamoneum Vitaliy Kolotylo, Alicja Synowiec, Kamil Piwowarek, Iwona Gientka, Marek Kieliszek // Appl Microbiol Biotechnol. 2025 Oct 16;109(1):228. doi: 10.1007/s00253-025-13606-y
- The frequently used industrial food process additive, microbial transglutaminase: boon or bane Lerner A, Benzvi C, Vojdani A (2025) // Nutrition Reviews, Volume 83, Issue 3, March 2025, Pages e1286–e1294, https://doi.org/10.1093/nutrit/nuae087
- Processed Food Additive Microbial Transglutaminase and Its Cross-Linked Gliadin Complexes Are Potential Public Health Concerns in Celiac Disease Lerner A., Matthias T. // Int. J. Mol. Sci. 2020, 21(3), 1127, DOI: 10.3390/ijms2103112
- Kieliszek M. Microbial transglutaminase in food biotechnology: from biochemical mechanisms to industrial applications. Applied Microbiology and Biotechnology, 2026.
- Properties and applications of microbial transglutaminase Yokoyama K., Nio N., Kikuchi Y. // Applied Microbiology and Biotechnology, 2004.
- Optimization of microencapsulation conditions of transglutaminase by freeze drying Hilal Isleroglu, Izzet Turker, Banu Koc, Mehmet Tokatli // J Food Sci Technol. 2019 Oct 16;56(11):4925–4937. doi: 10.1007/s13197-019-03962-9 https://pmc.ncbi.nlm.nih.gov /articles/PMC6828876
- Improving the performance of transglutaminase-crosslinked microparticles for enteric delivery Fernando Tello, Ana S. Prata, Rodney A.F. Rodrigues, etc // Food Research International Volume 88, Part A, October 2016, Pages 153-158 https://doi.org/10.1016/j.foodres.2016.02.020
Источник фото: 123rf.com
Автор материала – Ирина Правская, руководитель направления разработки «Константа ИТ» Материал подготовлен совместно с партнером комьюнити по...
В пятницу, 20 марта 2026 года прошел форум АПК 360, где принимало участие много именитых и известных отраслевых деятелей и...
Материал подготовлен совместно с комьюнити Digital4food и Ириной Правской, руководителем направления разработки «Константа ИТ» И вот момент...
Парейдолия - это распространенная зрительная иллюзия, при которой мозг, стремясь распознать знакомые образы, «дорисовывает» базовые...
Новинки Останкино (ТМ "Папа Может", "Останкино", "Коровино") на выставке ПРОДЭКСПО 2026 ...
Коллеги цифровизаторы-интеграторы, айтишники и все умеющие отличать штрих-коды от...
Уважаемые коллеги здравствуйте. скажите пожалуйста кто уже подал заявку на участие в пилотном...
ну или креазот и деготь вам на стол для вашей печени. Фото снято в ноябре 2025...
Здравствуйте. Остаётся щетина после обесволашивания. Пробовали увеличение циклов, замену бил,...
Здравствуйте, уважаемые! Посоветуйте, пожалуйста. Предлагают по 80000 рублей две термокамеры...
Добрый вечер всем. Когда то писал письмо в ВНИИМП по данным книгам, которые они издавали, на...